Εισαγωγή
Υπάρχουν περιορισμένα δεδομένα για τον ρόλο της χρόνιας λήψης ριφαξιμίνης στην κλινική έκβαση των ασθενών με μη αντιρροπούμενη κίρρωση (μη-ΑΚ).
Σκοπός
Να εκτιμηθεί ο προγνωστικός ρόλος της χρόνιας λήψης ριφαξιμίνης σε ασθενείς με μη-ΑΚ.
Μέθοδοι
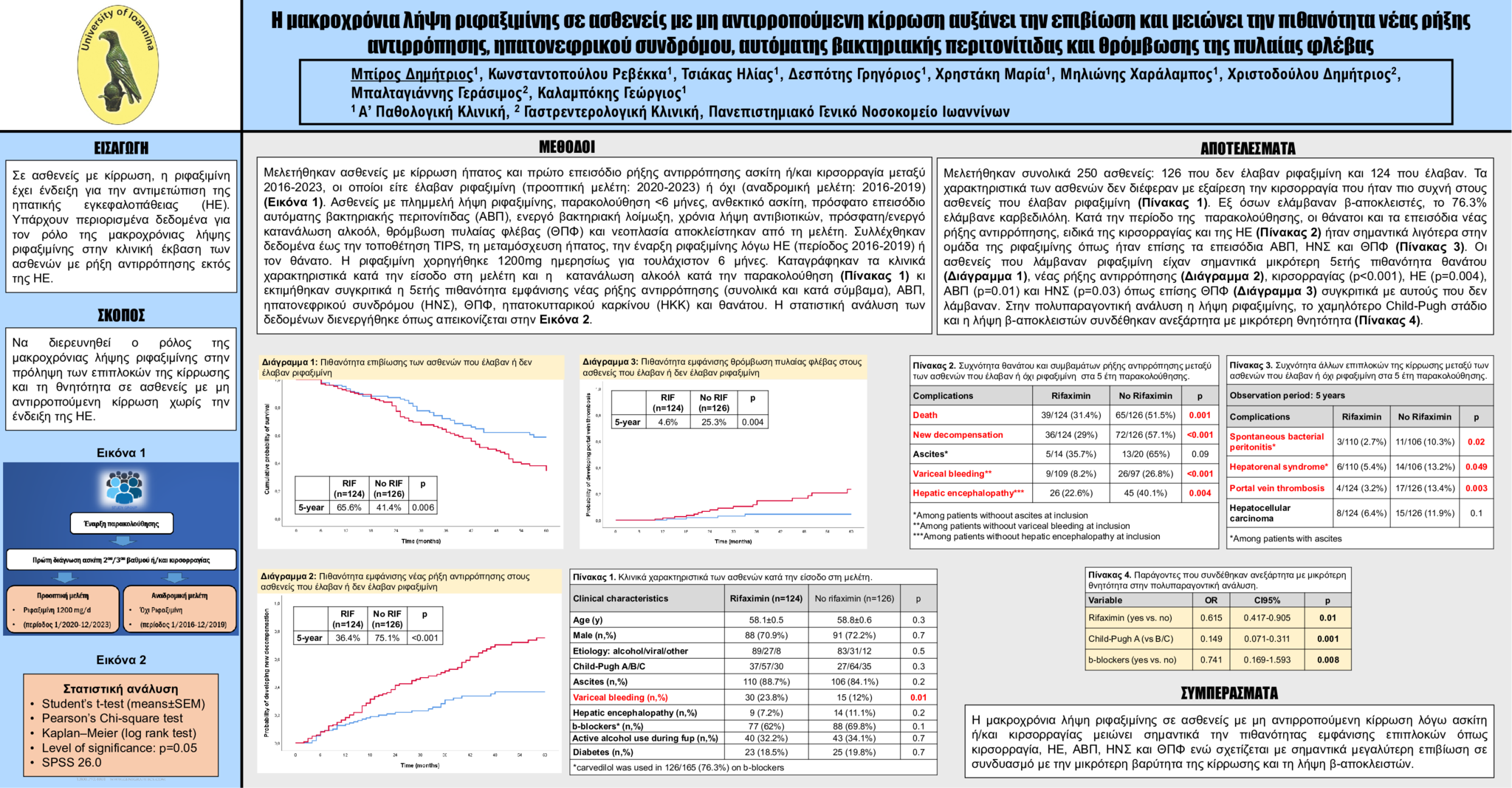
Το διάστημα 1/2020-12/2023, 124 ασθενείς εκτιμήθηκαν προοπτικά με ρήξη αντιρρόπησης (ασκίτης, κιρσορραγία, ηπατική εγκεφαλοπάθεια [ΗΕ] ή συνδυασμός αυτών) κι έλαβαν ριφαξιμίνη 1200 mg ημερησίως. Η κλινική έκβαση των ασθενών συγκρίθηκε με αυτή 126 ασθενών με μη-ΑΚ που εκτιμήθηκαν διαδοχικά το διάστημα 1/2016-12/2019. Αποκλείστηκαν ασθενείς με <6 μήνες παρακολούθηση, ασκίτη 1ου βαθμού, ασκίτη 2ου/3ου βαθμού μη ανταποκρινόμενο στη διουρητική αγωγή, προηγούμενο ιστορικό αυτόματης βακτηριακής περιτονίτιδας (ΑΒΠ), χρόνια λήψη αντιβιοτικής αγωγής, κρεατινίνη ορού >1.5mg/dl, πρόσφατη/ενεργό κατανάλωση αλκοόλ, θρόμβωση πυλαίας φλέβας (ΘΠΦ) και νεοπλασία. Καταγράφηκαν δεδομένα έως την τοποθέτηση διασφαγιτιδικής ενδοηπατικής πυλαιοσυστηματικής αναστόμωσης, τη μεταμόσχευση ήπατος, την τελευταία παρακολούθηση, την έναρξη ριφαξιμίνης λόγω ΗΕ (ασθενείς περιόδου 1/2016-12/2019), τον θάνατο ή τη λήξη της μελέτης. Εκτιμήθηκαν συγκριτικά (καμπύλες Kaplan-Meier, log-rank test) η πιθανότητα εμφάνισης νέας ρήξης αντιρρόπησης (συνολικά και κατά σύμβαμα), ΑΒΠ, ηπατονεφρικού συνδρόμου (ΗΝΣ), ΘΠΦ, ηπατοκυτταρικού καρκίνου (ΗΚΚ) και θανάτου στα 5 έτη. Επίσης, διερευνήθηκαν παράγοντες με ανεξάρτητη συσχέτιση με τη θνητότητα (Cox regression analysis).
Αποτελέσματα
Κατά την είσοδο στη μελέτη, οι ασθενείς που έλαβαν ριφαξιμίνη και αυτοί που δεν έλαβαν δεν διέφεραν όσον αφορά την ηλικία (58.1±0.5 έναντι 58.8±0.6 έτη;p=0.3), το φύλο (άρρεν: 70.9% έναντι 72.2%;p=0.7), την αιτιολογία της κίρρωσης (αλκοολική/ιογενής/άλλη αιτιολογία: 89/27/8 έναντι 83/31/12;p=0.5), την βαρύτητα της κίρρωσης (Child-Pugh A/B/C: 37/57/30 έναντι 27/64/35;p=0.3) και την συχνότητα του ασκίτη (88.7% έναντι 84.1%;p=0.2) και της ΗΕ (7.2% έναντι 11.1%;p=0.2) ενώ η συχνότητα κιρσορραγίας ήταν σημαντικά υψηλότερη στην ομάδα ασθενών που δεν έλαβε ριφαξιμίνη έναντι αυτής που έλαβε (23.8% έναντι 12%;p=0.01). Οι δύο ομάδες ασθενών δεν διέφεραν όσον αφορά τη λήψη β-αποκλειστών (62% έναντι 69.8%;p=0.1) την παρουσία σακχαρώδους διαβήτη (18.5% έναντι 19.8%;p=0.7) και την ενεργό κατανάλωση αλκοόλ στη διάρκεια της παρακολούθησης (32.2% έναντι 34.1%;p=0.7). Κανένας ασθενής δεν διέκοψε την ριφαξιμίνη λόγω ανεπιθύμητων ενεργειών. Ριφαξιμίνη λόγω ΗΕ χορηγήθηκε στην πορεία σε 13 ασθενείς (10.3%) της ομάδας που δεν λάμβανε. Μεταξύ των 165 ασθενών που λάμβαναν β-αποκλειστή, το 76.3% λάμβανε καρβεδιλόλη. Στα 5 έτη, οι ασθενείς που έλαβαν ριφαξιμίνη, συγκριτικά με αυτούς που δεν έλαβαν, εμφάνισαν σημαντικά μικρότερο ποσοστό νέων συμβαμάτων ρήξης αντιρρόπησης συνολικά (36/124 [29%]-65/126 [51.5%];p<0.001), κιρσορραγίας (9/109 [8.2%]-26/97 [26.8%];p<0.001), ΗΕ (26/115 22.6%]-45/112 [40.1%];p=0.004), ΑΒΠ (3/110 [2.7%]-11/106 [10.3%] μεταξύ των ασθενών με ασκίτη; p=0.02), ΗΝΣ (6/110 [5.4%]-14/106 [13.2%] μεταξύ των ασθενών με ασκίτη; p=0.049), ΘΠΦ (4/124 [3.2%]-17/126 [13.4%];p=0.003) και θανάτων (39/124 [31.4%]-65/126 [51.5%];p=0.001) ενώ δεν διέφερε σημαντικά το ποσοστό ΗΚΚ (8/124 [6.4%]-15/126 [11.9%];p=0.1). Στις καμπύλες Kaplan-Meier, οι ασθενείς που έλαβαν ριφαξιμίνη έναντι αυτών που δεν έλαβαν εμφάνισαν σημαντικά μικρότερη 5ετή πιθανότητα εμφάνισης νέας ρήξης αντιρρόπησης (36.4%-75.1%;p<0.001), κιρσορραγίας (12.9%-37.1%;p<0.001), ΗΕ (29.2%-59.7%;p=0.004), ΑΒΠ (4.1%-17.1%;p=0.01), ΗΝΣ (8.2%-25.3%;p=0.03), ΘΠΦ (4.6%-25.3%;p=0.004) και θνητότητας (41.4%-65.6%;p=0.006). Η λήψη ριφαξιμίνης (HR:0.615; CI:0.417-0.905; p=0.01) το Child-Pugh Α στάδιο έναντι των B/C (HR:0.149; CI:0.071-0.311; p=0.001) και η λήψη β-αποκλειστή (HR:0.741; CI:0.169-1.593; p=0.008) σχετίστηκαν ανεξάρτητα με χαμηλότερη θνητότητα.
Συμπεράσματα
Η χρόνια λήψη ριφαξιμίνης βελτιώνει σημαντικά την κλινική έκβαση των ασθενών με μη-ΑΚ συμπεριλαμβανομένης της εμφάνισης ΘΠΦ.
- 2 προβολές